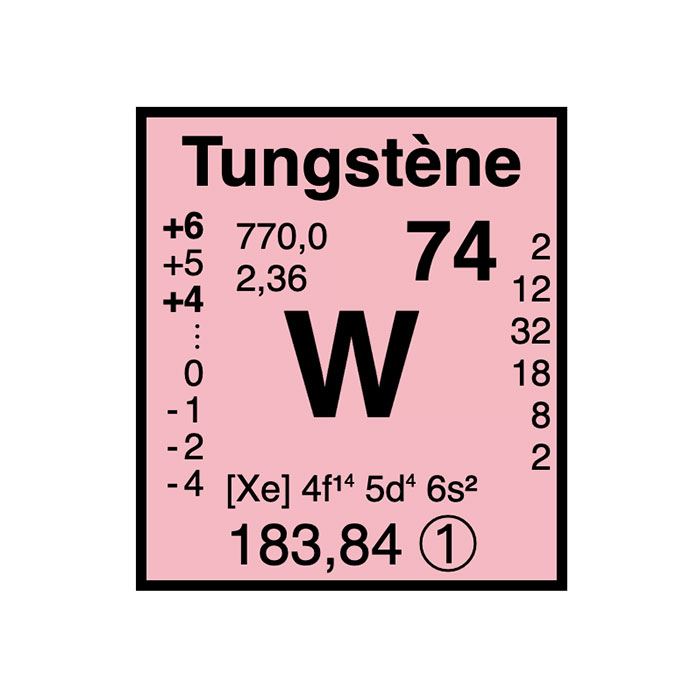
Características del Tungsteno
- Símbolo: W
- Masa atómica: 183,84 ± 0,01 u1
- Número CAS: 7440-33-7
- Configuración electrónica: [Xe]6s24f145d4
- Número atómico: 74
- Grupo: 6
- Bloque: Bloque d
- Familia de elementos: Metal de transición
- Electronegatividad: 2,36
- Punto de fusión: 3 422 °C


