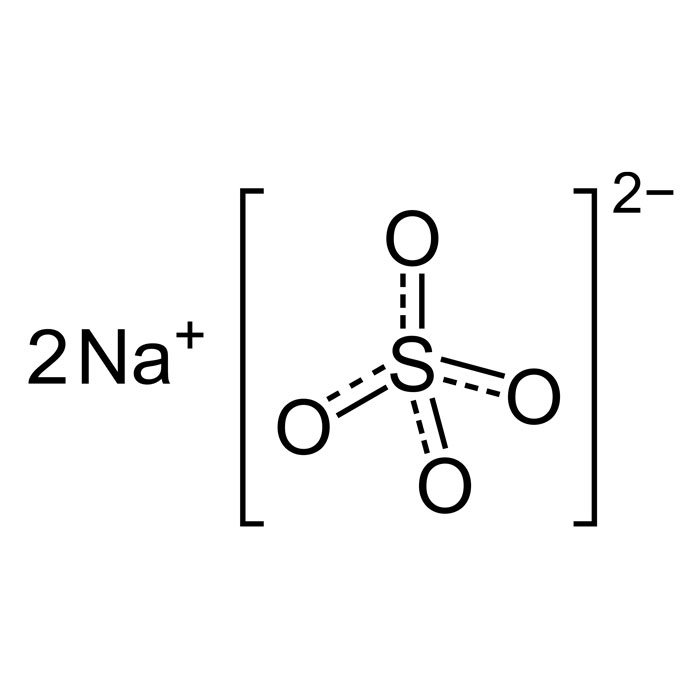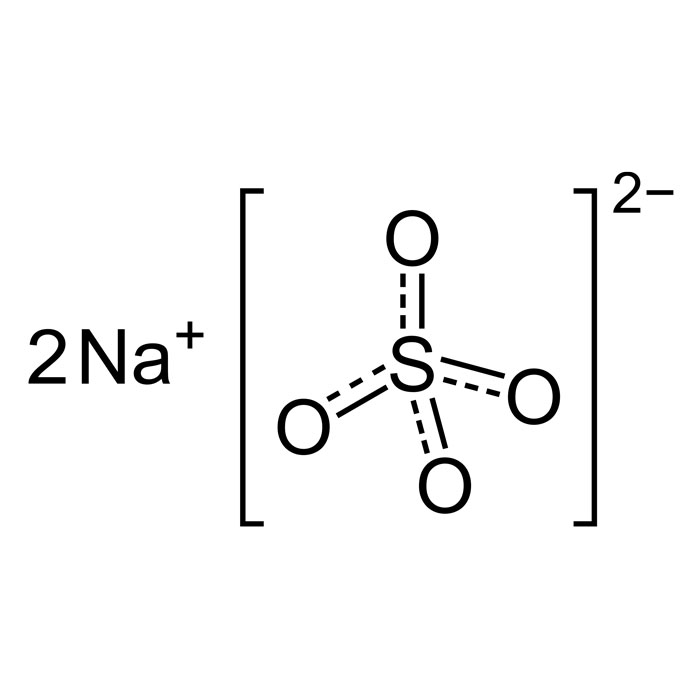
Características del sulfato de sodio
- Identificación del sulfato de sodio:
- Nombre UICPA: disodium sulfate
- Sinónimos: Sulfato disódico, sulfato de sodio anhidro, bisulfato de sodio, E514
- N° CAS: 7757-82-6
- N° ECHA: 100.028.928
- N° CE: 231-820-9
- Código ATC: A12CA02
- PubChem: 24436
- ChEBI: 32149
- FEMA: –
- SMILES:[O-]S(=O)(=O)[O-].[Na+].[Na+]
- InChl: 1S/2Na.H2O4S/c;;1-5(2,3)4/h;;(H2,1,2,3,4)/q2*+1;/p-2
Propiedades químicas:
- Fórmula: Na2SO4
- Masa molar: 142,04 g/mol
- pKa: –
Propiedades físicas:
- T° Fusión: 884 °C (anhidro); 32,38 °C (decahidrato)
- Solubilidad: 47,6 g·kg-1 (en agua a 0 °C); 427 g·kg-1 (en agua a 100 °C) para la celda romboédrica
Propiedades bioquímicas:
- Codones: –
- pH isoeléctrico: –
- Aminoácido esencial: –
- Ocurrencia en vertebrados: –
Propiedades ópticas:
- Poder rotatorio: –
Precauciones:
- SIMDUT: producto no controlado