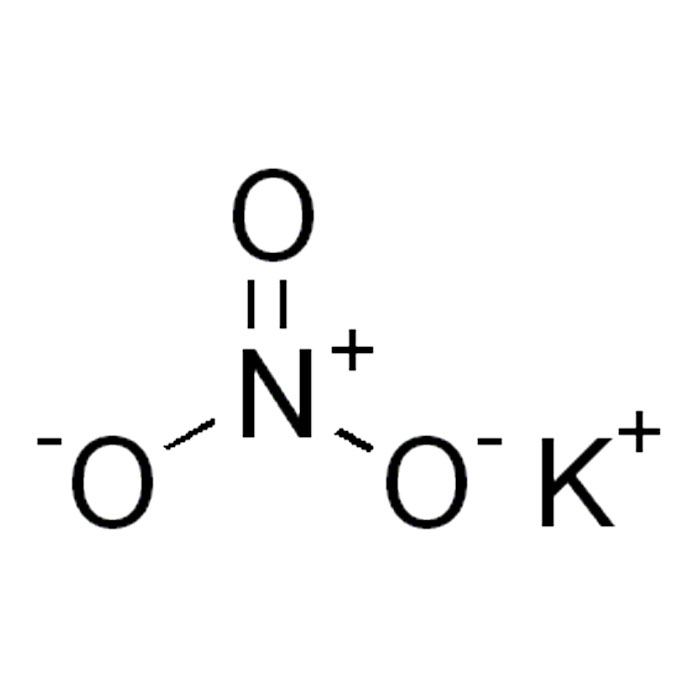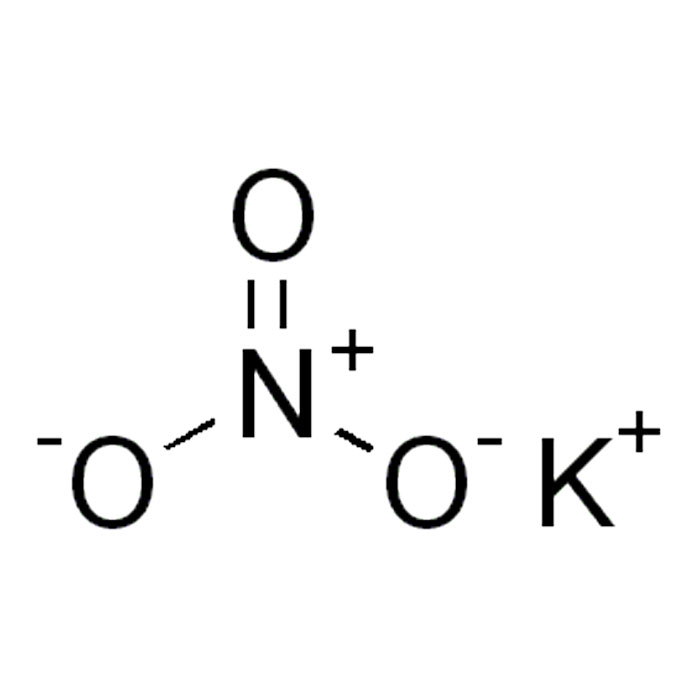
Características del nitrato de potasio
- Identificación del nitrato de potasio:
- Nombre UICPA: nitrato de potasio
- Sinónimos: salitre, nitro, nitrato de potasa, sal de piedra
- N° CAS: 7757-79-1
- N° ECHA: 100.028.926
- N° CE: 231-818-8
- Código ATC: –
- PubChem: 24434
- ChEBI: 63043
- FEMA: –
- SMILES:[N+](=O)([O-])[O-].[K+]
- InChl: 1S/K.NO3/c;2-1(3)4/q+1;-1
Propiedades químicas:
- Fórmula: KNO3
- Masa molar: 101,103 g/mol, de los cuales K = 38,67 %, N = 13,85 % y O = 47,47 %
- pKa: –
Propiedades físicas:
- T° Fusión: 333 a 334 °C
- Solubilidad: 35 g/100 ml; muy soluble en agua a 25 °C (357 g/L-1); 1,61 g/L-1 en alcohol al 90 %; insoluble en alcohol absoluto o etanol.
Propiedades bioquímicas:
- Codones: –
- pH isoeléctrico: –
- Aminoácido esencial: –
- Ocurrencia en vertebrados: –
Propiedades ópticas:
- Poder rotatorio: –
Precauciones:
- SIMDUT: Materia comburente; causa o favorece la combustión de otra materia liberando oxígeno; divulgación al 1,0 % según los criterios de clasificación