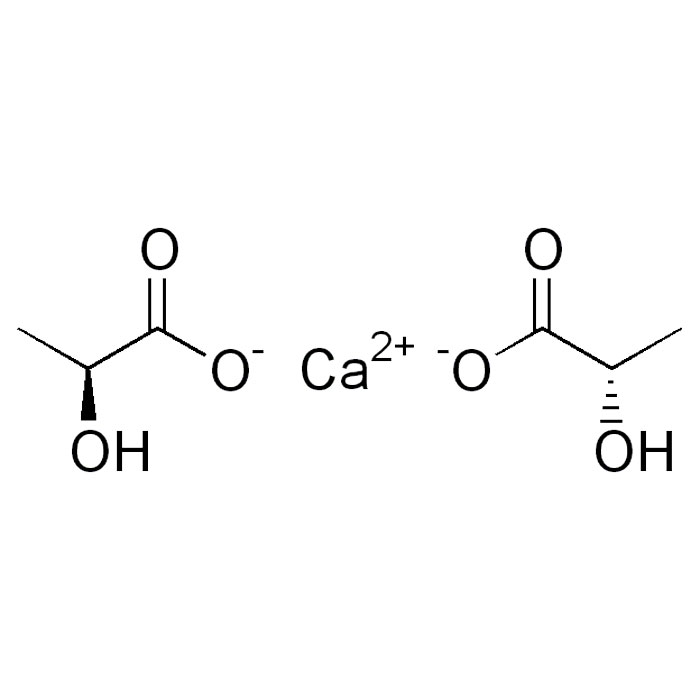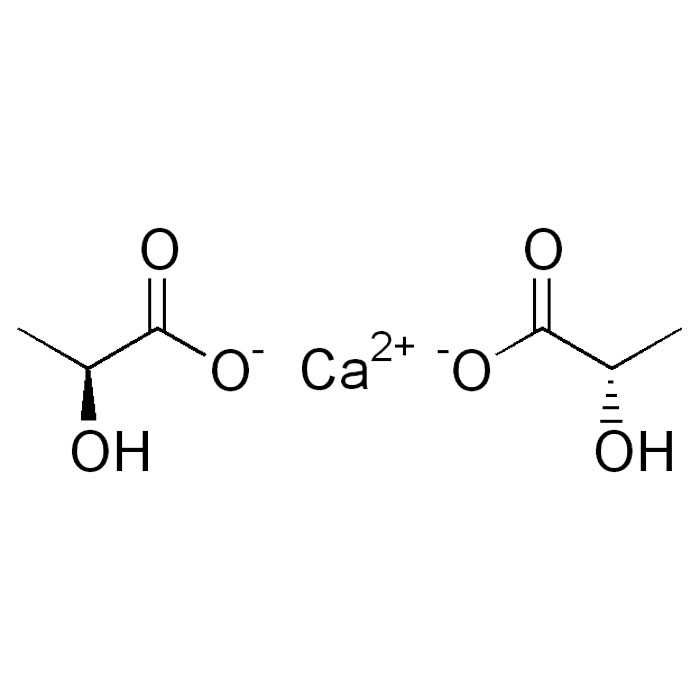
Características del lactato de calcio
- Identificación del lactato de calcio:
- Nombre IUPAC: calcio bis(2-hidroxipropanoato)
- Sinónimos: calfosano, dilactato de calcio y E327
- N° CAS: 814-80-2
- N° ECHA: 100.011.278
- N° CE: 212-406-7
- Código ATC: A12AA05
- PubChem: 13144
- ChEBI: –
- FEMA: –
- SMILES:CC(C(=O)[O-])O.CC(C(=O)[O-])O.[Ca+2]
- InChl: 1S/2C3H6O3.Ca/c2*1-2(4)3(5)6;/h2*2,4H,1H3,(H,5,6);/q;;+2/p-2
Propiedades químicas:
- Fórmula: C6H10CaO6
- Masa molar: 218,22 g/mol
- pKa: 6,0-8,5
Propiedades físicas:
- T° Fusión: 240 °C
- Solubilidad: insoluble en etanol y soluble en metanol.
Propiedades bioquímicas:
- Codones: –
- pH isoeléctrico: –
- Aminoácido esencial: –
- Ocurrencia en vertebrados: –
Propiedades ópticas:
- Poder rotatorio: –
Precauciones:
- SIMDUT: producto no inflamable.