Características del E513
- Identificación del E513:
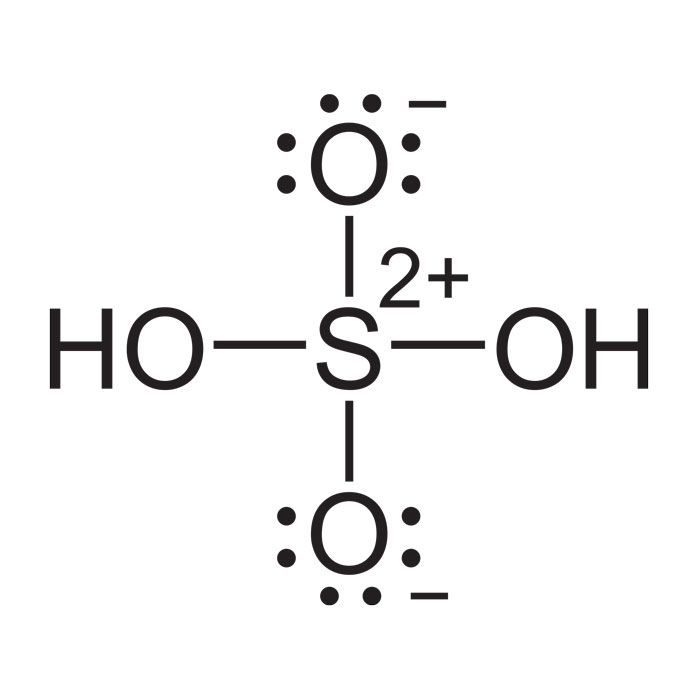
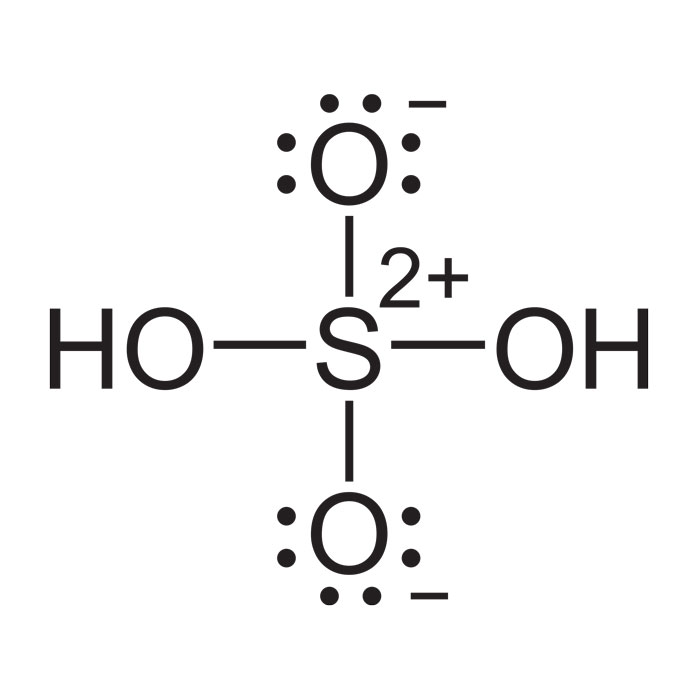
- Nombre UICPA: ácido sulfúrico
- Sinónimos: ácido sulfúrico concentrado, sulfato de hidrógeno, aceite de vitriolo, vitriolo, sulfuric acid
- N° CAS: 7664-93-9
- N° ECHA: 100.028.763
- N° CE: 231-639-5
- Código ATC:–
- PubChem: 1118
- ChEBI: 26836
- FEMA:–
- SMILES: OS(=O)(=O)O
- InChl: 1S/H2O4S/c1-5(2,3)4/h(H2,1,2,3,4)
Propiedades químicas:
- Fórmula: H2SO4 ; H2O4S
- Masa molar: 98,08 g/mol
- pKa: -3 ; 1,92 a 25 °C
Propiedades físicas:
- T° Fusión: 10 °C ; 10,31 °C
- Solubilidad: miscible con agua y alcohol
Propiedades bioquímicas:
- Codones:–
- pH isoeléctrico:–
- Aminoácido esencial:–
- Ocurrencia en vertebrados:–
Propiedades ópticas:
- Poder rotatorio:–
Precauciones:
- SIMDUT: D1A: Materia altamente tóxica con efectos inmediatos gravesLetalidad aguda: CL50 inhalación/4 h (ratón) = 160 mg/m3E: Materia corrosivaTransporte de mercancías peligrosas: clase 8