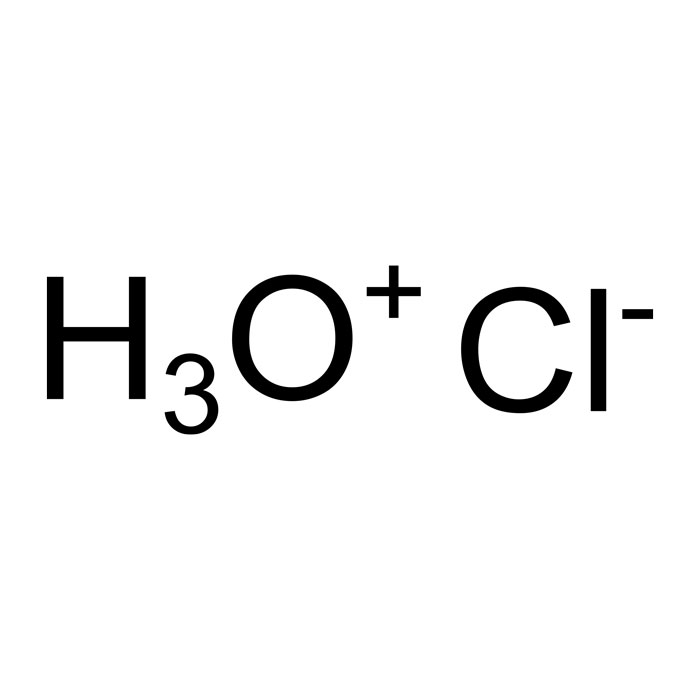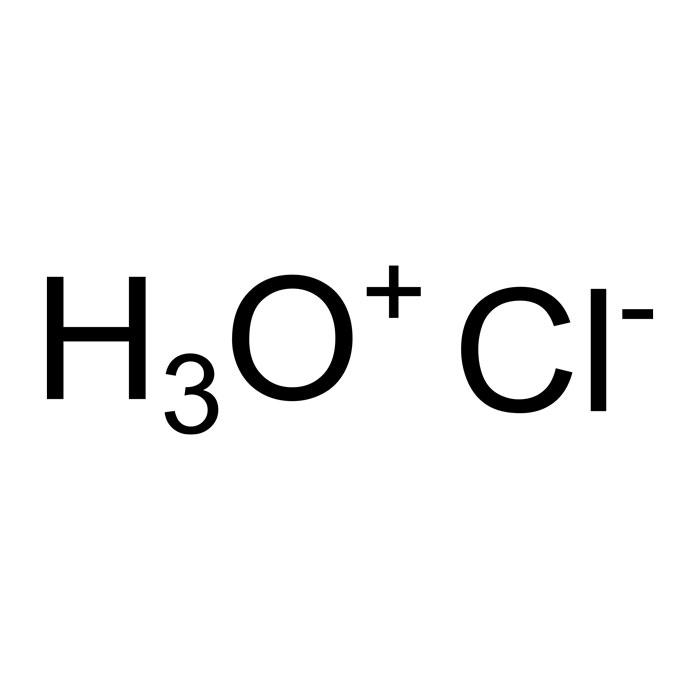
Características del E507
- Identificación del E507:
- Nombre UICPA: clorano
- Sinónimos: ácido clorhídrico, espíritu de sal, ácido hidroclórico, clorano, monohidrocloruro, cloruro de hidrógeno anhidro, ácido muriático
- N° CAS: 7647-01-0
- N° ECHA: 100.210.665
- N° CE: 231-595-7
- Código ATC: B05XA13
- PubChem: 313
- ChEBI: 17883
- FEMA:–
- SMILES: Cl
- InChl: 1S/ClH/h1H
Propiedades químicas:
- Fórmula: HCl (isómeros)
- Masa molar: 36,46 g/mol, donde H = 2,76 % y Cl = 97,23 %
- pKa: -6,3
Propiedades físicas:
- T° Fusión: -114,2 °C
- Solubilidad: Solubilidad en agua: 82,3 g/100 g de agua a 0 °C; 67,3 g/100 g de agua a 30 °C; 63,3 g/100 g de agua a 40 °C; 59,6 g/100 g de agua a 50 °C; 56,1 g/100 g de agua a 60 °C Solubilidad en metanol: 54,6 g/100 g de solución a -10 °C; 51,3 g/100 g de solución a 0 °C; 47 g/100 g de solución a 20 °C; 43 g/100 g de solución a 30 °C Solubilidad en etanol: 45,4 g/100 g de solución a 0 °C; 42,7 g/100 g de solución a 10 °C; 41 g/100 g de solución a 20 °C; 38,1 g/100 g de solución a 30 °C Solubilidad en éter: 37,52 g/100 g de solución a -10 °C; 35,6 g/100 g de solución a 0 °C; 24,9 g/100 g de solución a 20 °C; 19,47 g/100 g de solución a 30 °C
Propiedades bioquímicas:
- Codones:–
- pH isoeléctrico:–
- Aminoácido esencial:–
- Ocurrencia en vertebrados: presente en el jugo gástrico del estómago, y secretado por las células parietales de las glándulas epiteliales en una cantidad de hasta 2 L por día
Propiedades ópticas:
- Poder rotatorio:–
Precauciones:
- SIMDUT: H302 (nocivo en caso de ingestión); H315 (provoca irritación cutánea); H319 (provoca irritación ocular severa); H314 (provoca quemaduras graves en la piel y lesiones oculares graves)