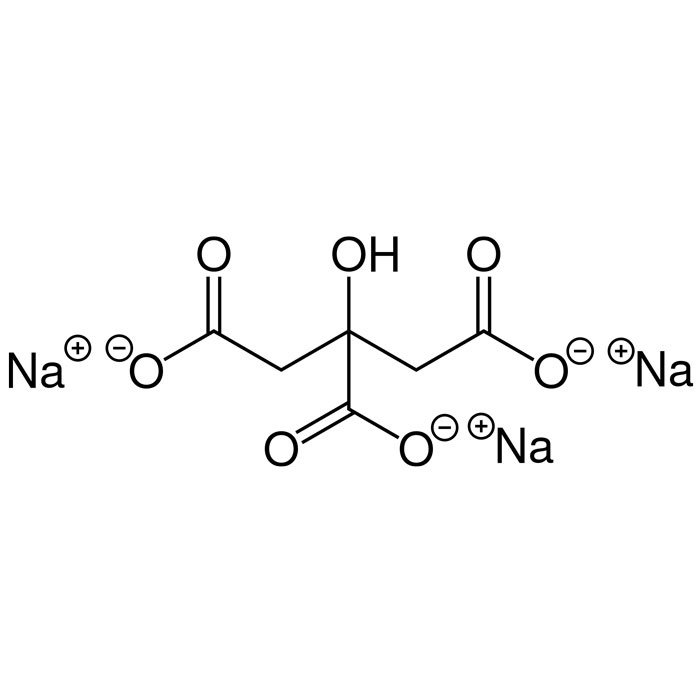
Características del citrato de sodio
- Identificación del citrato de sodio:
- Nombre UICPA: trisodio;2-hidroxipropano-1,2,3-tricarboxilato
- Sinónimos: citrato de sodio, citrato trisódico, citrato de sodio anhidro, citrosodina
- N° CAS: 68-04-2
- N° ECHA: 100.000.614
- N° CE: 200-675-3
- Código ATC: B05CB02
- PubChem: 6224
- ChEBI: 53258
- FEMA: 3026
- SMILES:C(C(=O)[O-])C(CC(=O)[O-])(C(=O)[O-])O.[Na+].[Na+].[Na+]
- InChl: 1S/C6H8O7.3Na/c7-3(8)1-6(13,5(11)12)2-4(9)10;;;/h13H,1-2H2,(H,7,8)(H,9,10)(H,11,12);;;/q;3*+1/p-3
Propiedades químicas:
- Fórmula: C6H5Na3O7 ; C6H5O7. 3Na
- Masa molar: 258,07 g/mol
- pKa: –
Propiedades físicas:
- T° Fusión: 300 °C
- Solubilidad: 425 g/l en agua a 25 °C
Propiedades bioquímicas:
- Codones: –
- pH isoeléctrico: –
- Aminoácido esencial: –
- Ocurrencia en vertebrados: –
Propiedades ópticas:
- Poder rotatorio: –
Precauciones:
- SIMDUT: polvo combustible.
