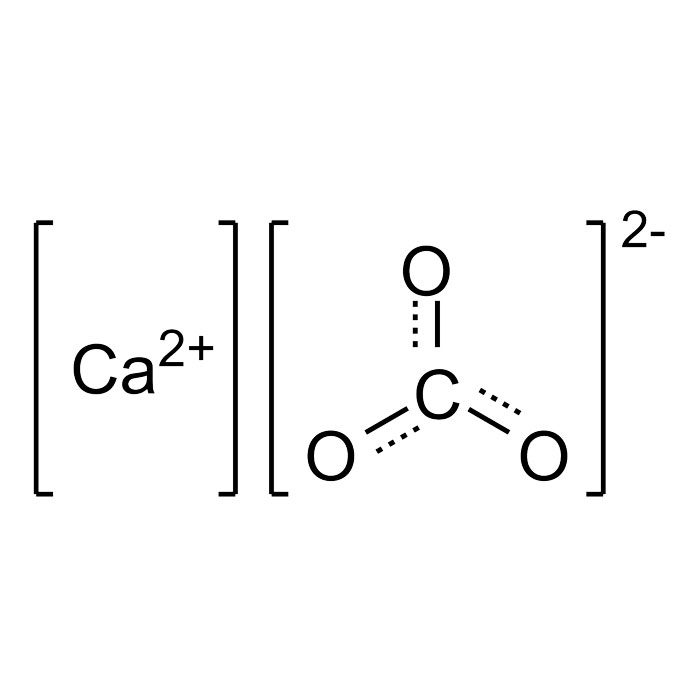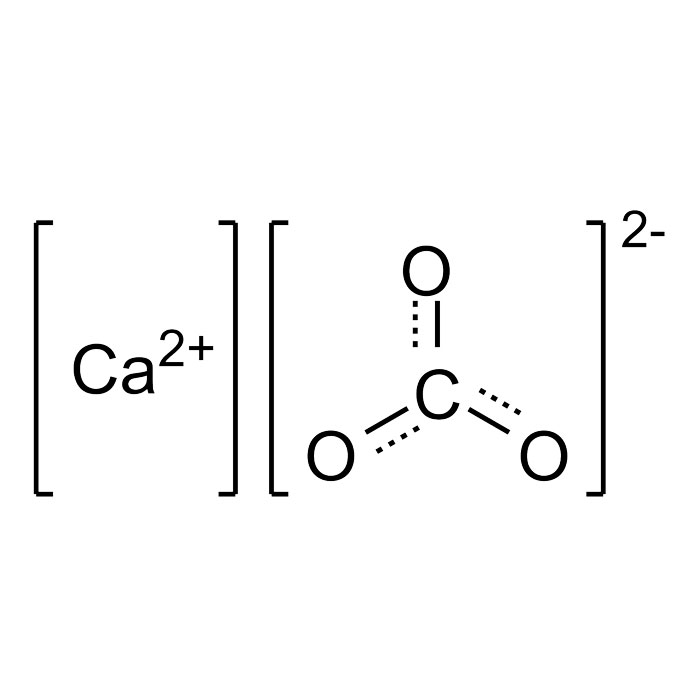
Características del carbonato de calcio
- Identificación del carbonato de calcio:
- Nombre UICPA: carbonato de calcio
- Sinónimos: carbonato de cal precipitado, calcium carbonate, aragonita, limestone, calcita, E 170, vaterita, chalk, CI pigment white 18, drop chalk, prepared chalk, whiting, english white, Paris white
- N° CAS: 471-34-1, 13397-26-7, 13701-58-1, 1317-65-3
- N° ECHA: 100.006.765
- N° CE: 207-439-9
- Código ATC: A02AC01, A12AA04
- PubChem: 10112
- ChEBI: 3311
- FEMA: –
- SMILES:C(=O)([O-])[O-].[Ca+2]
- InChl: 1S/CH2O3.Ca/c2-1(3)4;/h(H2,2,3,4);/q;+2/p-2
Propiedades químicas:
- Fórmula: CaCO3, CCaO3
- Masa molar: 100,09 g/mol
- pKa: 9
Propiedades físicas:
- T° Fusión: 825 °C
- Solubilidad: en agua: 14 mg L-1 a 20 °C, 0,013 g/L (a 25 °C)
Propiedades bioquímicas:
- Codones: –
- pH isoeléctrico: –
- Aminoácido esencial: –
- Ocurrencia en vertebrados: –
Propiedades ópticas:
- Poder rotatorio: –
Precauciones:
- SIMDUT: –